Цель. Оценить прогностическое значение локальных захватов (ЛЗ) после изоляции устьев легочных вен (ЛВ) у пациентов с непароксизмальной формой фибрилляции предсердий (ФП) на отдаленные результаты радиочастотной аблации (РЧА).
Материал и методы исследования. Исследование одноцентровое обсервационное проспективное. Общее количество пациентов 110. Всем выполнена первичная катетерная аблация по поводу непароксизмальной формы ФП. Во время операции оценивалась активность ЛВ и наличие ЛЗ. Пациенты, у которых ЛЗ после изоляции ЛВ встречались хотя бы в одной ЛВ, вошли в первую группу; больные, у которых ЛЗ отсутствовали - во вторую. Первая группа - 54 пациента, вторая группа - 56 пациентов. Группы больных не имели статистически значимых различий по основным показателям - полу, весу, возрасту, длительности анамнеза, объему левого предсердия и фракции выброса левого желудочка, а также по сопутствующей патологии. Характеристики проведенных операций - время РЧА и флюороскопии, длительность - между группами так же не имели статистически значимых различий.
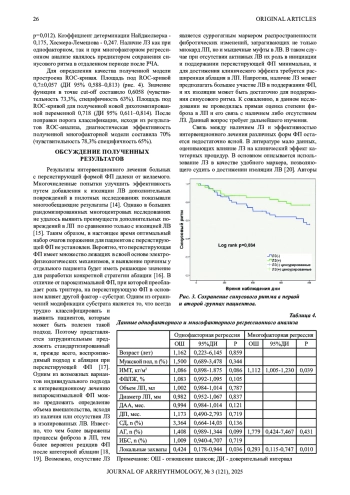
Результаты. Период наблюдения за больными составил в среднем 800 [286,5;800] дней. Среди всей когорты пациентов общая эффективность лечения составила 68,2% (75 пациентов из 110) с учетом повторных операций. В группе с ЛЗ синусовый ритм по истечении срока наблюдения сохранялся у 42 пациентов из 54 (77,7%), в группе без ЛЗ у 33 пациентов из 56 (58,9%). Различие является статистически значимым (отношение шансов 2,439 (95% доверительный интервал 1,060–5,615 p=0,034). Наличие ЛЗ при построении многофакторной логистической регрессионной модели является предиктором эффективности РЧА (χ2=14,710; р=0,012).
Заключение. В данном исследовании ЛЗ в ЛВ у пациентов с непароксизмальной формой ФП после выполнения катетерной изоляции ЛВ являлись предиктором улучшения отдаленных результатов радиочастотной аблации.
Идентификаторы и классификаторы
Фибрилляция предсердий (ФП) является наиболее распространённой аритмией в человеческой популяции, повышая риски инсульта и неблагоприятных сердечно-сосудистых исходов [1]. Эффективность лечения ФП далека от 100%, особенно при непароксизмальных формах [2]. Катетерная аблация, как показали рандомизированные клинические исследования, более эффективна, чем фармакологическое лечение, снижает риск рецидивов ФП и улучшает качество жизни пациентов. Также она может влиять на выживаемость пациентов с застойной сердечной недостаточностью [3-5].
Список литературы
1. Stylianos T, Edward P, Jonathan K, et al. 2024 European Heart Rhythm Association/Heart Rhythm Society/Asia Pacific Heart Rhythm Society/Latin American Heart Rhythm Society expert consensus statement on catheter and surgical ablation of atrial fibrillation. EP Europace 2024;26(4). DOI: 10.1093/europace/euae043
2. Chander S, Kumari R, Luhana S, et al. Antiarrhythmic drug therapy and catheter ablation in patients with paroxysmal or persistent atrial fibrillation: a systematic review and meta-analysis. BMC Cardiovasc Disord. 2024;24(1): 32. DOI: 10.1186/s12872-024-03983-z
3. Packer D, Mark D, Robb R, et al. Effect of Catheter Ablation vs Antiarrhythmic Drug Therapy on Mortality, Stroke, Bleeding, and Cardiac Arrest Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA. 2019;321(13): 1261-1274. DOI: 10.1001/jama.2019.0693
4. Sohns C, Fox H, Marrouche N, et al. Catheter Ablation in End-Stage Heart Failure with Atrial Fibrillation. N Engl J Med. 2023;389(15): 1380-1389. DOI: 10.1056/NEJMoa2306037
5. Базылев ВВ, Козлов АВ, Дурманов СС, и др. Качество жизни после этапного интервенционного или одномоментного хирургического лечения пароксизмальной формы фибрилляции предсердий и ишемической болезни сердца. Анналы аритмологии. 2021;18(1): 53-61.
Bazylev VV, Kozlov AV, Durmanov SS, et al. Quality of life after staged interventional or simultaneous surgical treatment of paroxysmal atrial fibrillation and coronary heart disease. Annaly aritmologii. 2021;18(1): 53-61. (In Russ.). DOI: 10.15275/annaritmol.2021.1
6. Haissaguerre M, Jais P, Shah D, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med. 1998;339(10): 659-66. DOI: 10.1056/NEJM199809033391003
7. Bredeloux P, Pasqualin C, Bordy R, et al. Automatic Activity Arising in Cardiac Muscle Sleeves of the Pulmonary Vein. Biomolecules. 2021;12(1): 23. DOI: 10.3390/biom12010023
8. Teh A, Kistler P, Lee G, et al. Electroanatomic properties of the pulmonary veins: slowed conduction, low voltage and altered refractoriness in AF patients. J Cardiovasc Electrophysiol. 2011;22(10): 1083-91. DOI: 10.1111/j.1540-8167.2011.02089.x
9. Базылев ВВ, Козлов АВ, Дурманов С.С. Наличие локальных захватов миокарда легочных вен после радиочастотной изоляции улучшает результат лечения у пациентов с пароксизмальной формой фибрилляции предсердий. Вестник аритмологии. 2023;30(4): 5-12.
Bazylev VV, Kozlov AV, Durmanov SS. The presence of local captures of the myocardium of the pulmonary veins after radiofrequency isolation improves the outcome of treatment in patients with paroxysmal atrial fibrillation. Journal of Arrhythmology. 2023;30(4): 5-12. (In Russ.). DOI: 10.35336/VA-1186
10. Попылькова ОВ, Дурманов СС, Базылев ВВ, и др. Варфарин против прямых оральных антикоагулянтов: как отличается степень коагуляции во время катетерной аблации фибрилляции предсердий Вестник аритмологии. 2022;29(3): 13-20.
Popylkova OV, Durmanov SS, Bazylev VV, et al. Warfarin versus direct oral anticoagulants: how the degree of coagulation differs during catheter ablation of atrial fibrillation. Journal of Arrhythmology. 2022;29(3): 13-20. (In Russ.). DOI: 10.35336/VA-2022-3-02
11. Phlips T, El Haddad M, Duytschaever M, et al. Improving procedural and one-year outcome after contact force-guided pulmonary vein isolation: the role of interlesion distance, ablation index, and contact force variability in the ‘CLOSE’-protocol, EP Europace. 2018;20(3): 419-427. DOI: 10.1093/europace/eux376
12. Михайлов ЕН, Гасымова НЗ, Айвазьян СА, и др. Факторы, ассоциированные с эффективностью радиочастотной катетерной аблации фибрилляции предсердий: мнение специалистов, применяющих технологию “индекс аблации”. Вестник аритмологии. 2020;27(3): 9-24.
Mikhaylov EN, Gasimova NZ, Ayvazyan SA, et al. Factors associated with the efficacy of atrial fibrillation radiofrequency catheter ablation: opinion of the specialists who use the “ablation index” module. Journal of Arrhythmology. 2020;27(3): 9-24. (In Russ.). DOI: 10.35336/VA-2020-3-9-24
13. Seitz J, Bars C, Théodore G, et al. AF Ablation Guided by Spatiotemporal Electrogram Dispersion Without Pulmonary Vein Isolation: A Wholly Patient-Tailored Approach. J Am Coll Cardiol. 2017;69(3): 303-321. DOI: 10.1016/j.jacc.2016.10.065
14. Griffin M, Calvert P, Gupta D. Persistent Atrial Fibrillation Ablation: Ongoing Challenges Defining the Target Population and Substrate. Curr Treat Options Cardio Med. 2023;25(10): 461-475. DOI: 10.1007/s11936-023-01011-5
15. Cheng-ming M, Ye-jian H, Wen-wen L, et al. Optimal Catheter Ablation Strategy for Patients with Persistent Atrial. Fibrillation and Heart Failure: A Retrospective Study. Cardiology Research and Practice. 2022;1: 1-7. DOI: 10.1155/2022/3002391
16. Dhillon GS, Honarbakhsh S, Graham A, et al. Driver characteristics associated with structurally and electrically remodeled atria in persistent atrial fibrillation. Heart Rhythm O2. 2022;3(6Part A): 631-638. DOI: 10.1016/j.hroo.2022.09.016
17. Palamà Z, Nesti M, Robles AG, et al. Tailoring the Ablative Strategy for Atrial Fibrillation: A State-of-the-Art Review. Cardiol Res Pract. 2022;2022: 9295326. DOI: 10.1155/2022/9295326
18. Kwon S, Choi EK, Lee SR, et al. The left atrial low-voltage area and persistent atrial fibrillation treated with pulmonary vein isolation alone. European Heart Journal. 2022;43(Supplement2). DOI: 10.1093/eurheartj/ehac544.464
19. Ma J, Chen Q, Ma S. Left atrial fibrosis in atrial fibrillation: Mechanisms, clinical evaluation and management. J Cell Mol Med. 2021;25(6): 2764-2775. DOI: 10.1111/jcmm.16350
20. Yang F, Raiszaden F, Fisher J, et al. Pulmonary Vein Isolation: Making the Most of Local Vein Capture with Exit Block. The Journal of Innovations in Cardiac Rhythm Management 2015;6: 2078-2084. DOI: 10.19102/icrm.2015.060705
21. Babak A, Kauffman CB, Lynady C, et al. Pulmonary vein capture is a predictor for long-term success of stand-alone pulmonary vein isolation with cryoballoon ablation in patients with persistent atrial fibrillation. Front Cardiovasc Med. 2024;10: 1150378. DOI: 10.3389/fcvm.2023.1150378
22. Issa ZF, Miller JM, Zipes DP. Clinical Arrhythmology and Electrophysiology.1st ed. Philadelphia: Saunders; 2009:242.
23. Squara F, Liuba I, Chik W, et al. Loss of local capture of the pulmonary vein myocardium after antral isolation: prevalence and clinical significance. J Cardiovasc Electrophysiol. 2015;26(3): 242-250.
Выпуск
Другие статьи выпуска
Среди исследований проблемы ЭКГ-стратификации риска внезапной сердечной смерти и жизнеугрожающих желудочковых аритмий представляют интерес новые подходы к анализу ЭКГ-данных и маркеров электрической нестабильности миокарда на их основе. В частности, заслуживают внимания показатели, получаемые с помощью векторного, частотного и нелинейного анализа ЭКГ-данных, продемонстрировавшие ценность в качестве предикторов опасных желудочковых аритмий и внезапной сердечной смерти.
В статье представлены современные методы анестезиологического пособия, используемые в ходе выполнения таких интервенционных и хирургических вмешательств как имплантация кардиостимуляторов, устройств сердечной ресинхронизирующей терапии, кардиовертеров-дефибрилляторов и проведения катетерной аблации. Обсуждаются преимущества, недостатки и проблемные вопросы анестезии в зависимости от типа вмешательства и состояния пациента. На основании проанализированных данных делается вывод о том, что анестезия в ходе вмешательств у пациентов аритмологического профиля является общемировой практикой и подчеркивается положительное влияние методов анестезии на качество и безопасность выполняемых процедур.
Статья посвящена анализу выбора устройства для сердечной ресинхронизирующей терапии, опираясь на стратификацию риска внезапной сердечной смерти. Рассматриваются возможные методы диагностики и клинико-анамнестические данные, а также их роль в прогнозировании аритмогенных событий и принятии решений об имплантации. Обсуждаются различия в подходах к имплантации у пациентов с ишемической и неишемической кардиомиопатией, значимость комбинированной оценки риска и применение прогностических моделей. Рассматриваются нерешенные вопросы оптимального отбора пациентов, сроков оценки эффективности СРТ и возможных стратегий имплантации устройств с учетом экономических и клинических факторов.
Представлен впервые зарегистрированный на территории Республики Казахстан клинический случай ребенка с редким митохондриальным заболеванием - синдромом Кернса-Сейра, у которого в связи с развитием полной атриовентрикулярной блокады был имплантирован электрокардиостимулятор. Обсуждаются вопросы диагностики и тактики ведения.
Цель. Оценить влияние предсердной стимуляции (atrial pacing, AP) на развитие предсердных экстрасистол (ПЭС) и эпизодов наджелудочковой тахикардии у пациентов с двухкамерными электрокардиостимуляторами (ЭКС).
Материал и методы исследования. В исследование включены 97 пациентов, перенесших имплантацию двухкамерных ЭКС. Проведен анализ 169 контрольных осмотров в период от 1 до 20 месяцев после операции. Оценивались показатели предсердной стимуляции, групповые ПЭС и эпизоды наджелудочковой тахикардии. Исходные данные обрабатывались в Microsoft Excel и Access, статистический анализ проведён в Jupyter Notebook (Python 3. x).
Результаты. Установлена умеренная положительная корреляция между ПЭС и эпизодами наджелудочковой тахикардии (ρ =0,623, p<0,001). В группе AP ≥ 91% отмечено снижение частоты наджелудочковой тахикардии (предсердной тахикардии / фибрилляции предсердий) продолжительностью более 24 часов (p=0,060). Логистическая регрессия показала значимое снижение риска наджелудочковой тахикардии продолжительностью более 24 часов при AP 51-90% (отношение рисков 0,31, p=0,002).
Заключение. Высокий уровень предсердной стимуляции может снижать риск длительных эпизодов наджелудочковой тахикардии, однако влияние предсердной стимуляции ЭКС на эпизоды ПЭС не достигло статистической значимости.
Цель. Сравнить непосредственные и отдаленные результаты катетерного лечения фибрилляции предсердий (ФП) после криобаллонной аблации (КБА) легочных вен (ЛВ) с использованием криобаллона второго поколения и радиочастотной аблации (РЧА) ЛВ вен на навигационной системе с катетером c датчиком давления «катетерткань» c использованием модуля Ablation Index (AI).
Материал и методы исследования. В исследование были включены 199 пациентов, направленных на процедуру катетерной изоляции ЛВ в период 2018-2021 гг. Пациенты были распределены на две группы: исследуемая группа - 110 пациентов, у которых изоляция ЛВ достигалась путем РЧА с помощью катетера с модулем AI; контрольная группа - 89 пациентов, подвергшиеся КБА ЛВ криобаллоном второго поколения. Период наблюдения был ограничен 36 месяцами, средний период наблюдения составил 27,9±14,2 месяцев.
Результаты. Трехлетняя эффективность КБА и РЧА ЛВ является сопоставимой (свобода от предсердных тахиаритмий в группе РЧА - 0,61±0,05, в группе КБА - 0,62±0,05, (Log-Rank test, p = 0,896)) при сходной частоте и структуре осложнений (3,6% (4) vs. 4,5 (4), p=0,759). Частота рецидивов ФП в «слепом» периоде достоверно ниже в группе РЧА (1,8% (2) vs. 9,0% (8) в группе РЧА, p=0,045). Длительность оперативного вмешательства значимо меньше в группе криоаблации (РЧА 92,7±20,9 мин, КБА 83,9±19,6 мин, p=0,005). Потребность в повторном оперативном вмешательстве сопоставима для обеих групп (РЧА 21,8% (n=24), КБА 30,3% (n=27), p=0,171).
Заключение. Сравнительный анализ трехлетней эффективности радиочастотной антральной изоляции легочных вен катетером с использованием модуля AI продемонстрировал сопоставимость результатов с аблацией криобаллоном второго поколения. При этом в «слепом» периоде наблюдения группа РЧА характеризовалась статистически значимым снижением частоты рецидивов предсердной тахиаритмии по сравнению с группой КБА.
Цель. Изучить значение индекса аблации (ИА) в рамках катетерной аблации (КА) желудочковых тахикардий (ЖТ) без применения флюороскопии у пациентов с хронической сердечной недостаточностью
Материал и методы исследования. В проспективном исследовании 47 пациентам с ишемической болезнью сердца, хронической сердечной недостаточностью была выполнена КА устойчивых ЖТ. Оценивались интраоперационные параметры КА, в том числе величина среднего индекса аблации. Оценивался факт индукции аритмии после серии радиочастотных (РЧ) воздействий. Также проводилась оценка рецидива ЖТ. Срок наблюдения составил 12 месяцев.
Результаты. Во время оперативного вмешательства после нанесения РЧ-воздействий индукция аритмии была неосуществима у 100% пациентов. Спустя 12 месяцев наблюдения свобода от аритмии составила 84,8%. Пациенты без рецидива ЖТ имели статистически значимо больший показатель среднего ИА (612 [522,5;683,5]), чем с рецидивом ЖТ (7 (15,2%) пациентов) (438 [416,5;462]) (p=0,001). Также проводилась оценка возможности прогнозирования рецидива ЖТ в зависимости от величины среднего ИА. Было получено, что при величине среднего ИА больше или равном 473, риск рецидива ЖТ ниже (р=0,001).
Заключение. ИА может быть использован в качестве параметра контроля эффективного РЧ-воздействия в рамках проведения КА ЖТ наряду с другими детерминантами, используемыми в настоящее время.
Цель. Разработать прогностическую модель и балльную шкалу вероятности развития кардиомиопатии (КАА), ассоциированной с идиопатическими желудочковыми аритмиями (ЖА) у детей.
Материал и методы исследования. В исследование было включено 492 ребенка в возрасте от 1 до 17 лет с идиопатическими ЖА. Для создания прогностической модели была сформирована обучающая выборка (n=392), для валидации - тестовая выборка (n=100). Поиск независимых предикторов осуществлялся методом бинарной логистической регрессии, баллы для каждого предиктора устанавливались на основании показателя оценки шансов.
Результаты. Было установлено, что площадь поверхности тела ≥ 1,7 м2 увеличивает шансы развития КАА в 4,9 раза (1 балл), длительность предэктопического интервала желудочковой экстрасистолы < 434 мс - в 3,7 раза (1 балл), плотность ЖА 25-29% - в 8,4 раза (2 балла), плотность ЖА 30-34% - в 11,3 раза (3 балла), плотность ЖА ≥35% - в 17,2 раза (4 балла). Методом ROC анализа была определена специфичность суммы баллов. При сумме баллов до 2 определялась низкая вероятность (специфичность <48,1%), при сумме баллов 3-4 - средняя вероятность (специфичность 67,5-81,8%), при сумме баллов 5-6 - высокая вероятность развития КАА (специфичность >95,1%). AUC шкалы прогноза развития КАА составила 0,805±0,037 (95% ДИ: 0,732-0,878), p<0,001. AUC шкалы прогноза развития КАА у тестовой группы составила 0,893±0,034 (95% ДИ: 0,827-0,96), p<0,001. Разность площади ROC-кривой суммы баллов обучающей и тестовой групп составила 0,088±0,05. Площади под ROC-кривыми были сопоставимы (p=0,078).
Заключение. В ходе исследования были выявлены независимые предикторы развития КАА у детей с идиопатическими ЖА. На основании полученных предикторов была разработана шкала вероятности развития КАА, использование которой позволит рутинно оценивать вероятность развития КАА и сформировать персонализированный подход к наблюдению и лечению каждого ребенка с идиопатическими ЖА.
Цель. Оценка влияния сопутствующих заболеваний и аритмического анамнеза на вольтажные характеристики левого предсердия у пациентов с персистирующей фибрилляцией предсердий (ФП).
Материал и методы исследования. В исследование было включено 50 пациентов с персистирующей ФП, направленных на первичную радиочастотную аблацию. Всем пациентам выполнялось вольтажное картирование левого предсердия. Вольтажные карты состояли как минимум из 2000 точек, среднее количество точек 2128±104. Области с амплитудой биполярного сигнала 0,1-0,5 мВ относили к области низкого вольтажа (НВ), области с амплитудой биполярного сигнала менее 0,1 мВ расценивали, как область очень низкого вольтажа. Для каждой карты был рассчитан НВ% и процент очень низкого вольтажа.
Результаты. Мы выявили статистически значимую заметную корреляцию НВ% с возрастом (p<0,001 r=0,720), женским полом (p=0,016) и длительностью анамнеза на момент старта персистирования (p<0,001, r=0,503). На основании полученных нами данных для прогнозирования НВ% была разработана оригинальная шкала. Шкала включает: возраст, женский пол, длительность аритмического анамнеза на момент старта персистирования. При возрасте более 65 лет присваивался 1 балл, пациентам женского пола присваивался 1 балл, при длительности аритмического анамнеза на момент старта персистирования более 4 месяцев 1 балл, в остальных случаях 0 баллов. Количество баллов по данной шкале показало высокую корреляцию с НВ% (p<0,001 r=0,768). Шкала получила название ВЖД-ритм (Возраст, Женский пол, Длительность анамнеза на момент старта персистирования).
Заключение. Возраст, женский пол, и длительность аритмического анамнеза на момент старта персистирования являются предикторами процента сниженного вольтажа левого предсердия у пациентов с персистирующей ФП. Предложенная оригинальная шкала ВЖД-ритм может использоваться для прогнозирования объема сниженного вольтажа у пациентов с персистирующей ФП.
Издательство
- Издательство
- ТД ИНКАРТ
- Регион
- Россия, Санкт-Петербург
- Почтовый адрес
- Россия, 194214, Санкт-Петербург, Выборгское шоссе, д. 22А
- Юр. адрес
- 190068, г Санкт-Петербург, Адмиралтейский р-н, пер Бойцова, д 4, помещ 3Н офис 1
- ФИО
- Катковник Илья Владимирович (ГЕНЕРАЛЬНЫЙ ДИРЕКТОР)
- Контактный телефон
- +7 (___) _______